medical
根据《医疗器械监督管理条例》(国务院令第680号)、《医疗器械生产监督管理办法》(原国家食品药品监督管理总局令第7号)和原国家食品药品监督管理总局《关于发布医疗器械生产企业质量管理体系年度自查报告编写指南的通告》(2016年第76号),已实施《医疗器械生产质量管理规范》的第二、三类医疗器械生产企业应当定期按照医疗器械生产质量管理规范的要求,对质量管理体系运行情况进行全面自查,并于每年年底前向所在地省、自治区、直辖市药品监督管理部门提交年度自查报告。
截至目前,我省辖区内仍有部分第二、三类医疗器械生产企业未提交2020年度自查报告,现予以通报(附件1)。
请省局有关分局按照《医疗器械监督管理条例》第六十八条,对上述企业进行处罚并开展全项目监督检查,于8月10日前将监督检查和处罚情况集中上报省局医疗器械化妆品监管处(附件2)。
附件:
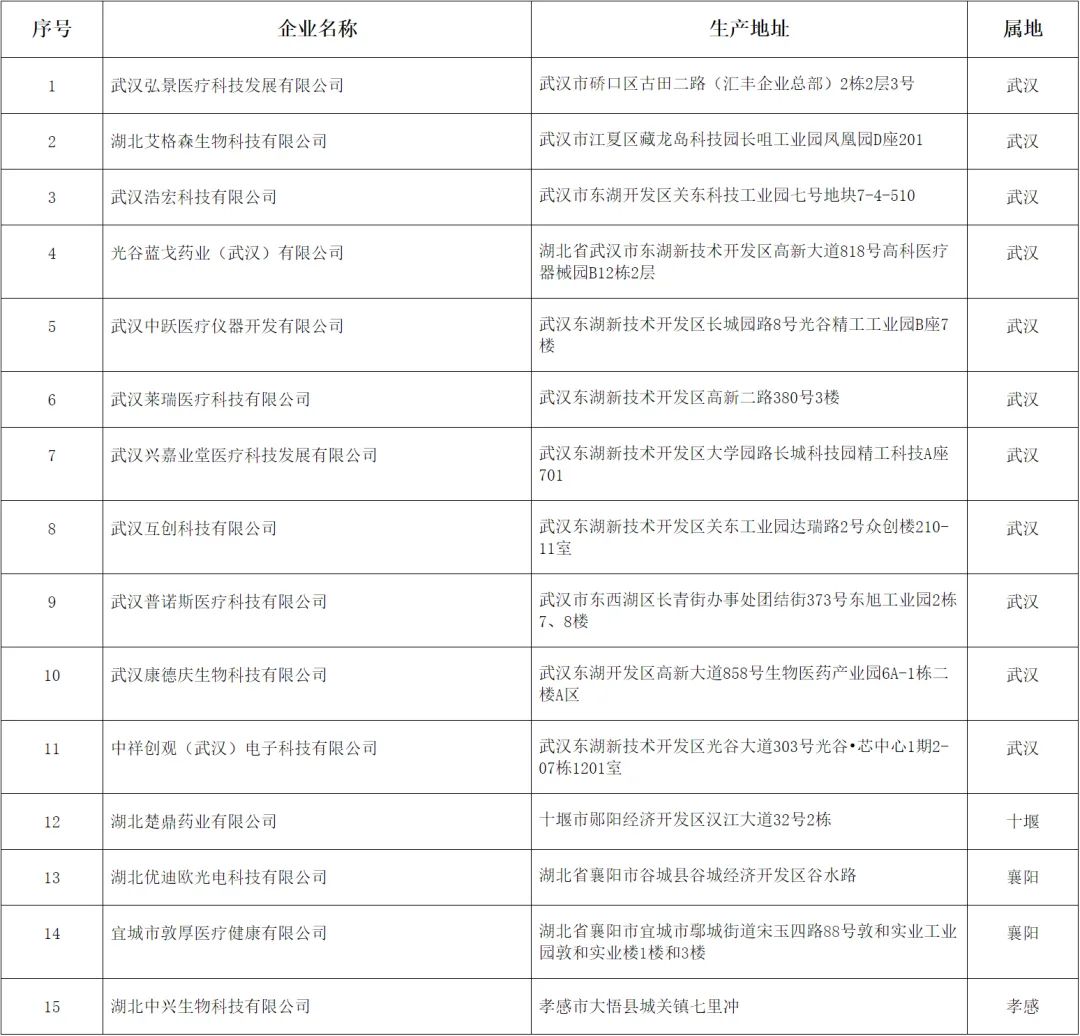
1.未提交2020年度自查报告第二、三类医疗器械生产企业名单
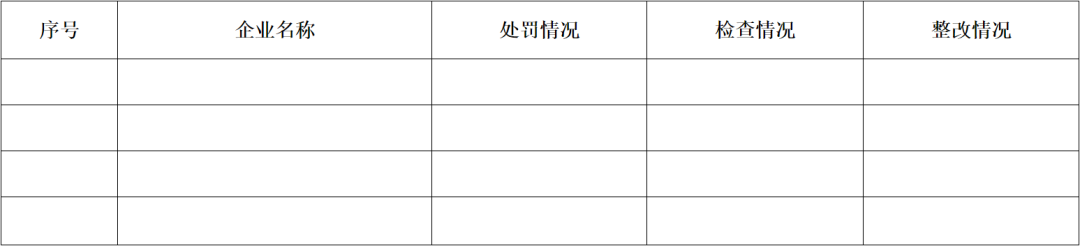
2.未提交2020年度自查报告第二、三类医疗器械生产企业检查和处罚情况
湖北省药品监督管理局
2021年6月24日
附件1
未提交2020年度自查报告
第二、三类医疗器械生产企业名单
附件2
未提交2020年度自查报告
第二、三类医疗器械生产企业
检查和处罚情况